Ligand (koordinačná chémia)

Ligandy[1] alebo adendy[1] (niekedy označované ako L) sú v koordinačnej chémii atómy alebo atómové skupiny (t.j. ióny alebo molekuly) koordinované okolo centrálneho atómu komplexu koordinačnej zlúčeniny (čiže sú naň viazané koordinačnou väzbou[2]).[1][3] Spravidla sú to donory elektrónov, ktoré sa skladajú z nekovových atómov.[4] Ligandy sú teda spravidla Lewisove bázy.[4]
Klasifikácia
[upraviť | upraviť zdroj]Existuje všeobecne veľké množstvo ligandov, ktoré je možné kategorizovať mnohými spôsobmi. Jeden zo spôsobov je napríklad podľa zložitosti molekuly:[4]
- monoatómové ligandy – ligandy zložené z jediného atómu, napríklad F- alebo S2-
- polyatómové monocentrické ligandy – ligandy, ktoré okrem väzbového atómu obsahujú len atómy viazané priamo na tento atóm, napríklad CN- alebo NO2-
- polyatómové polycentrické ligandy – zvyčajne veľké organické molekuly, ktoré obsahujú väčší počet atómov, napríklad étery (R2O) alebo alkylamíny (NR3)
Alternatívne je ligandy možné klasifikovať podľa ich náboja:[1]
- neutrálne ligandy, napríklad NH3 alebo H2O
- aniónové ligandy, napríklad OH- alebo Cl-
- katiónové ligandy, napríklad NO+
Chelácia
[upraviť | upraviť zdroj]Niektoré ligandy sa môžu na centrálny atóm viazať viac než jednou väzbou, takže ďalším spôsobom kategorizácie môže byť počet väzieb, ktoré ligand tvorí. Z tohto hľadiska možno rozlišovať ligandy napríklad nasledovne:[4]
- monodentátne ligandy – tvoria len jednu väzbu, napríklad Cl- (tieto ligandy môžu tvoriť viac väzieb, ak sú prítomné v komplexoch s viac než jedným centrálnym atómom, vtedy vystupujú ako mostíkové atómy)
- bidentátne ligandy – tvoria dve väzby, napríklad etyléndiamín
- tridentátne ligandy – tvoria tri väzby, napríklad 1,4,7-trioxacyklononán
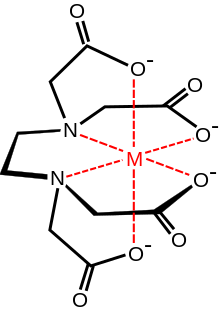
- polydentátne ligandy – tvoria viac ako tri väzby, napríklad kyselina etyléndiamínotetraoctová (EDTA), schopná tvoriť až 6 väzieb s jedným centrálnym atómom
Namiesto latinského základu „dentátny“ (od dentis, zub) sa niekedy používajú slová funkčný, donorový alebo väzbový (napr. jednodonorové alebo dvojfunkčné ligandy).[1]
Ligandy, ktoré tvoria viac ako jednu väzbu, sa označujú ako chelačné činidlá. Komplexy, ktoré tvoria, sa potom označujú ako cheláty.[4]
Referencie
[upraviť | upraviť zdroj]- ↑ a b c d e ligandy. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 429.
- ↑ koordinačná väzba. In: Encyclopaedia Beliana online [1]
- ↑ koordinačné zlúčeniny. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 386.
- ↑ a b c d e ČERNÁK, Juraj. Úvod do koordinačnej chémie [online]. Univerzita Jozefa Šafárika v Košiciach, 2011, [cit. 2023-06-12]. Dostupné online.